Vanilina: Origem, Propriedades e Produção
Originalmente publicado em Química Nova na Escola, v. 32, n. 4, 2010
Edição: Leila Cardoso TeruyaCoordenação: Guilherme Andrade Marson
|
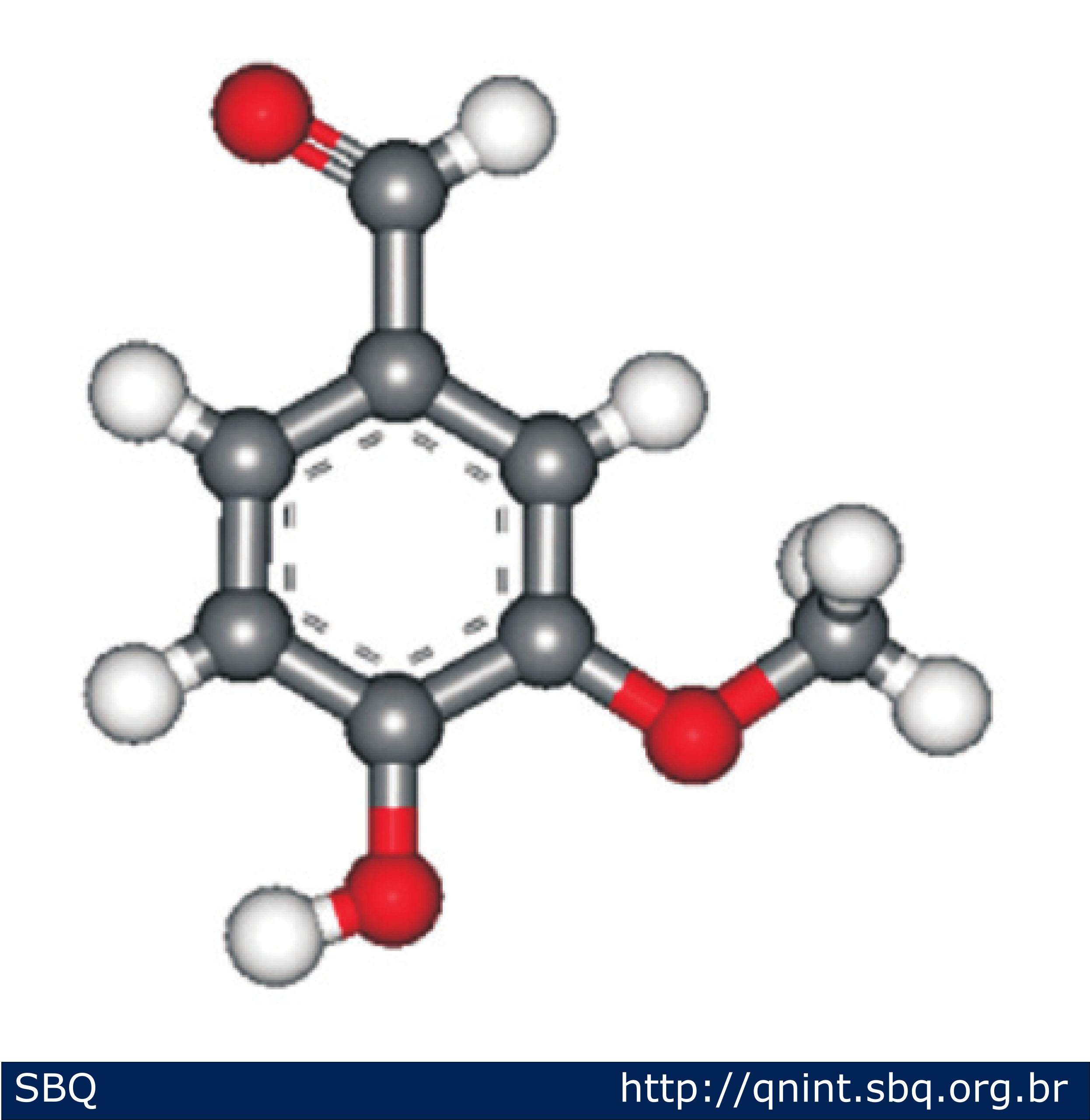
A molécula-alvo deste trabalho pode ser denominada usualmente como vanilina ou, por meio das regras da IUPAC, como 4-hidróxi-3-metoxibenzaldeído, sendo tradicionalmente conhecida como aroma de baunilha. É um composto cristalino de cor branca, solúvel em clorofórmio e éter. Possui peso molecular de 152,14 g.mol-1 e fórmula química (CH3O)(OH)C6H3CHO (Figura 1).
|
|
Figura 1: Estrutura química da vanilina. As diferentes cores das esferas representam os diferentes átomos presentes na molécula: hidrogênio (brancas), carbono (cinzas) e oxigênio (vermelhas) (Almeida e Ferreira, 2008). |
|
Origem e propriedades
De acordo com Pacheco, Junior e Morgado (2007):
“A vanilina é obtida tradicionalmente da vagem de uma orquídea tropical, a Vanilla planifolia [Figura 2] fazendo dela a única orquídea de interesse comercial fora do contexto ornamental. A publicação deste gênero de orquídea foi feita pela primeira vez, seguindo o sistema de Linneus, por Miller, em seu “Gardener’s Dictionary”, datado de 1754, com o nome latinizado de Vanilla”. (p. 46)
|
|
Figura 2: Foto da orquídea Vanilla planifólia (Ortobotanico, 2008). |
|
A vanilina já era cultivada e extraída da Vanilla planifolia pelos astecas muito antes da chegada do conquistador espanhol Hernán Cortés em 1519 que, por sua vez, além de introduzir outros produtos de importância financeira na Europa oriundos do Novo Mundo, tais como o corante cochonilha e o cacau, também introduziu a vanilina (Courteur e Burreson, 2006). Entretanto, o cultivo dessa orquídea não foi realizado com sucesso em clima europeu e, ainda hoje, são consideradas plantas de cultivo difícil. Esse fato deve-se principalmente à polinização a ser realizada por insetos que não existem na Europa.
O maior produtor mundial de vanilina natural extraída da Vanilla planifolia é Madagascar, seguida por outros países como México, Tahiti e Indonésia (Bythrow, 2005).
Segundo Lomascolo (1999), mais de 12.000 toneladas de vanilina são produzidas por ano. Desse total, apenas 1% é extraída da planta, sendo o restante sintetizado. Os custos da vanilina natural oscilam entre US$ 1.200,00 e 4.000,00 por quilo, em contraste com o preço da vanilina sintética, cujo quilo custa menos de US$ 15,00.
|
|
Aplicações
A vanilina é um dos aromatizantes mais importantes, sendo largamente utilizado em alimentos, bebidas, perfumes e fármacos (Clark, 1990).
Existem várias espécies do gênero Vanilla, que crescem em locais diferentes e, consequentemente, produzem aromas que possuem leves variações. O aroma extraído da Vanilla fragrans é conhecido por possuir a melhor qualidade (Bourbon) para preparações alimentares como sorvetes, bolos, chocolates e bebidas. Os aromas extraídos da Vanilla tahitensis (Sul do Pacífico), Vanilla java (Indonésia) e Vanilla pompana (Antilhas) são utilizados em tabacos, sabonetes, perfumes e medicamentos (Almeida e Ferreira, 2008).
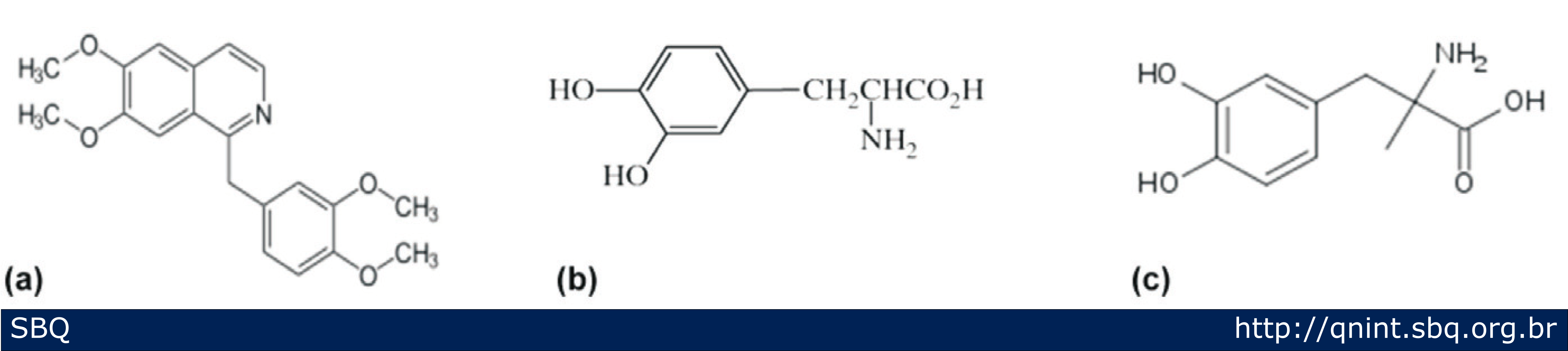
Aproximadamente 50% da produção mundial de vanilina sintética são usados como intermediário para síntese de herbicidas, agentes antiespumantes ou drogas tais como: papaverina, L-dopa, L-metildopa e agentes antimicrobianos (Figura 3). A vanilina também é utilizada para desodorizantes de ambientes e ceras para pisos e assoalhos (Almeida e Ferreira, 2008).
|
|
Figura 3: (a) Estrutura química da papaverina, (b) estrutura química da L-dopa e (c) estrutura química da L-metildopa. |
|
A vanilina possui propriedades antimicrobianas e antioxidantes. O fato de o fenol e seus derivados possuírem ação antimicrobiana é conhecido desde 1800, quando o cirurgião Joseph Lister utilizou fenol para reduzir infecção em incisões cirúrgicas. O fenol e seus derivados lesam as células microbianas pela alteração da permeabilidade seletiva da membrana citoplasmática, causando uma perda das substâncias intracelulares vitais. Esses compostos também desnaturam proteínas como as enzimas (Pelczar e cols., 1997).
As propriedades antioxidantes da vanilina devem-se ao fato de esta interagir com espécies radicalares, evitando, dessa forma, os processos oxidativos (Angelo e Jorge, 2007).
Tais características justificam o amplo uso da vanilina em alimentos na condição de conservantes. Ainda assim, o efeito antimicrobiano da vanilina bem como de vários outros extratos vegetais ainda não é totalmente compreendido (Antoniolli e cols., 2004). Além disso, algumas pesquisas ilustram o seu potencial antimutagênico (Maurya e cols., 2007).
|
|
Produção da vanilina natural
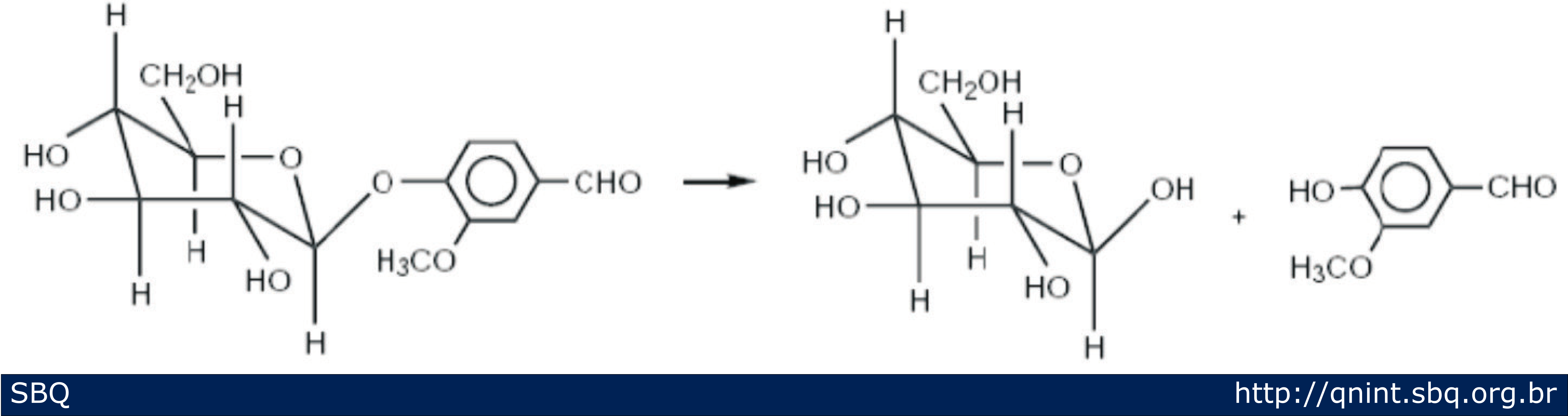
A produção natural de vanilina é realizada por meio da colheita e maturação das vagens da orquídea. A vanilina encontra-se nas vagens sob a forma de gluco-vanilina, sendo que nessas condições não possui o aroma característico de baunilha. No entanto, após o processo de maturação que envolve a secagem e umificação das vagens e que pode durar até seis meses para ocorrer, a gluco-vanilina é hidrolizada enzimaticamente em glucose e vanilina (Figura 4). O conteúdo de vanilina extraído por esse processo é de aproximadamente 2,5% em massa (Hocking, 1997; Lampman e cols, 1977).
|
|
Figura 4: Esquema ilustrativo da hidrólise enzimática de gluco-vanilina em glucose e vanilina (Maurya e cols., 2007).
|
A vanilina natural também pode ser obtida mediante um processo de extração com etanol (60% v/v) em temperaturas brandas ou por meio da extração com fluidos quentes, em que as vagens são adicionadas sobre grades situadas em tanques de aço, nos quais o solvente é recirculado por um período de aproximadamente duas semanas (Greener Industry, 2008). A extração com etanol das vagens ainda é o processo mais vantajoso para a obtenção da vanilina (Hocking, 1997).
As pessoas que trabalham com a extração de vanilina podem ser acometidas por uma enfermidade denominada vanilismo (Almeida e Ferreira, 2008). Esta é uma doença ocupacional que se caracteriza por provocar erupções cutâneas, irritações na pele e na membrana da mucosa nasal, insônia, dor de cabeça, menstruação excessiva e irritação da bexiga (Kerber, 2005).
Teoricamente a vanilina sintética não possui diferença em relação à vanilina natural. Entretanto, na prática, existe diferença em relação ao cheiro e flavor. Essa evidência é relacionada ao fato de a vanilina natural ser o resultado de vários compostos extraídos que não existem na vanilina sintética (Mukhopadhyay, 2005).
Segundo Pacheco, Júnior e Morgado (2007):
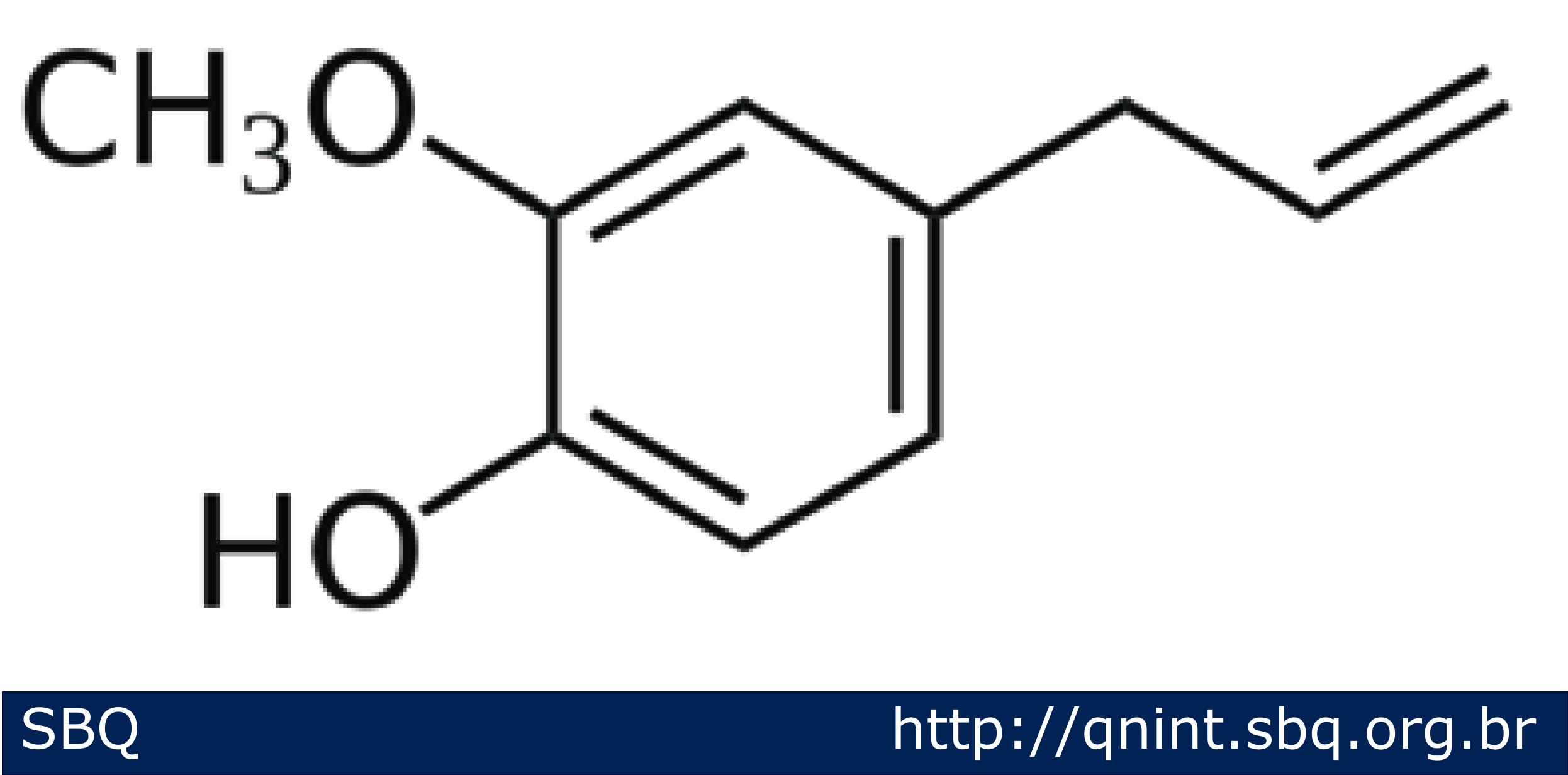
“Os custos elevados, somados aos pequenos rendimentos da produção de vanilina natural, estimularam a pesquisa por rotas de produção de vanilina sintética. Dessa forma, em 1874-1875, menos de vinte anos após seu isolamento e caracterização, a molécula de vanilina foi sintetizada a partir do eugenol tornando-se disponível comercialmente na França e Estados Unidos por 176,00 dólares por quilo (Hocking, 1997). O eugenol (encontrado no óleo de cravo) [Figura 5] continuou a ser utilizado como material de partida para a síntese de vanilina até 1920”. (p. 46-47)
|
Figura 5: Estrutura química do eugenol. Embora, a produção de vanilina por essa rota sintética possuir alto rendimento, esta consumia grandes quantidades de reagentes, o que desmotivou a produção da molécula por esse método. Mais tarde, a vanilina passou a ser sintetizada a partir da lignina contida no licor negro (Kortekaas e cols, 1998).
O licor negro é um resíduo das indústrias de papel e celulose que possui conteúdo de sólidos dissolvidos e uma grande diversidade de substâncias químicas oriundas da degradação de lignina (fenóis de baixa e alta massa molar e de toxicidade reconhecida) e polissacarídeos. A hipótese de que a vanilina poderia ser sintetizada a partir de substratos constituídos de lignina foi realizada por meio de uma publicação anônima em 1875 (Hocking, 1997).
A produção industrial de vanilina a partir da lignina contida no licor negro começou nos Estados Unidos em 1936 com a Salvo Chemical Corp. e a Marathon Paper Mills Co. de Wisconsin, utilizando a tecnologia desenvolvida por Tomlinson e Hibbert (Kortekaas e cols, 1998). Um ano depois, a Howard Smith Paper Mills Ltd. desenvolveu a primeira planta de produção de vanilina em grande escala no Canadá. Estudos realizados pela Ontario Pulp and Paper, em 1940, levaram à construção da segunda planta de produção de vanilina, chegando a uma produção de 227.000 Kg/ano em 1945 (Hocking, 1997).
Embora a produção de vanilina a partir do licor negro ter sido parcialmente motivada pelo interesse em reduzir o conteúdo de ligninas, açúcares e, consequentemente, a demanda bioquímica de oxigênio (DBO) desse rejeito, o processo possuía muitos inconvenientes como o fato de gerar um grande volume de resíduos tóxicos. Para produzir 1 kg de vanilina, eram utilizados 160 kg de líquidos cáusticos e gerados 150 kg de outras substâncias sem importância comercial e de reconhecido caráter tóxico (Hocking, 1997; Furukawa e cols., 1998; Greener Industry, 2008). Esse fator acabou levando ao fechamento das plantas no Canadá e nos EUA no fim da década de 1980 e início de 1990 (Hocking, 1997).
Atualmente, a maior parte da vanilina sintética é produzida por meio do uso de precursores derivados do petróleo. Os precursores oriundos da indústria petroquímica mais utilizados são o guaiacol e o p-cresol (Mukhopadhyay, 2005). Tais rotas vêm sendo mais usuais, pois elas são mais econômicas em relação às rotas que utilizam lignina e geram menos efluentes devido aos rendimentos das reações serem maiores (Hocking, 1997).
|
|
Produção da vanilina por meio de processos biotecnológicos
O aumento da população mundial impulsionou o crescimento de mercados especialmente voltados à produção de alimentos. Concomitante ao aumento do consumo de alimentos, encontra-se o aumento da demanda por aditivos alimentares, tais como a vanilina.
De acordo com o International Programs Center (U.S. Census Bureau), no mês de julho de 2010, estimou-se que a população mundial estava em mais de seis bilhões e oitocentas e cinquenta milhões de pessoas (Internacional Programs, 2010). Para suprir as necessidades da população, a inserção e o desenvolvimento de produtos sintéticos foram necessários devido ao fato de grande parte da superfície do planeta já ter sido ocupada pela agricultura. Apesar de os produtos sintéticos terem tornado-se imprescindíveis para o sustento da população mundial, existe um movimento crescente que impulsiona o consumo de produtos naturais (Furukawa e cols., 1998). Dessa forma, a vanilina sintética produzida de forma rentável e menos poluente por meio de precursores derivados do petróleo se confronta com o fato de utilizar compostos não renováveis para sua produção e, ainda, o de ser um produto sintético. Para contornar o dilema entre a grande demanda necessária dessa molécula e de se caracterizar como um produto sintético, a biotecnologia vem se mostrando como uma promissora solução.
Diversas publicações vêm demonstrando as formas de produção biotecnológica de vanilina. De acordo com Daugsch e Pastore (2005), quando essa molécula é produzida por meio de processos biotecnológicos, ela é considerada um produto natural, pois é oriunda de compostos de fontes renováveis e com custos relativamente baixos se comparados ao processo de extração da vanilina natural. Ainda segundo os autores citados, a produção biotecnológica da vanilina ocorre mediante o uso de extratos enzimáticos brutos ou enzimas purificadas produzidas principalmente por microrganismos ou plantas ou ainda por culturas de células.
Dentre os diversos compostos utilizados como precursores para a produção biotecnológica da vanilina, é possível citar a vanilil-amina, que pode ser extraída da pimenta. O estudo de Lesage-Meessen e cols. (1997) demonstrou que a vanilil-amina pode ser convertida em vanilina por meio da ação da enzima álcool vanililoxidase (EC 1.1.3.38).
Outra molécula que vem sendo intensamente estudada como precursora para a produção biotecnológica da vanilina é o ácido ferúlico que, por sua vez, é o componente majoritário da lignina. É válido ressaltar que a lignina, logo após a celulose, é a substância orgânica mais abundante da natureza. Dentro desse contexto, diversos fungos e bactérias capazes de biodegradar o ácido ferúlico vêm sendo isolados e estudados com o objetivo principal de se compreender os complexos mecanismos que envolvem a biodegradação da lignina e, consequentemente, a dos compostos fenólicos que a constituem. O ácido ferúlico também é encontrado em quantidades significativas na parede celular de exemplares importantes para a agricultura, tais como arroz, trigo, milho e beterraba (Narbad e Gasson, 1998).
Outros compostos fenólicos obtidos por meio de fontes naturais também podem ser utilizados para a produção biotecnológica de vanilina como, por exemplo, o ácido vanílico. O ácido vanílico também vem sendo citado em algumas publicações como composto intermediário formado antes da produção de vanilina a partir do ácido ferúlico. Alguns autores, tais como Lesage-Meessen e colaboradores (1996) e Stentelaire e colaboradores (2000), ilustraram a obtenção rentável de vanilina a partir de ácido vanílico, utilizando o fungo Pycnoporus cinnabarinus. Esse fungo não ocorre no hemisfério sul, porém é da mesma família que o Pycnoporus sanguineus, conhecido popularmente no Brasil como “orelha de pau” (Pacheco, Morgado e Furigo Júnior, 2008).
|
|
Aplicação do tema no ensino de química
Tomando como base as diretrizes sugeridas pelo Ministério da Educação, por meio dos Parâmetros Curriculares Nacionais para o Ensino Médio, o ensino dos saberes, de um modo geral, deve se desenvolver como algo que não envolva a simples memorização de ideias, leituras ou discursos. O aprendizado desses saberes exige vivência e atividade não só do tipo experimental, mas de caráter ativo, possibilitando a incorporação de procedimentos e valores associados à prática científica (MEC/SEMTEC, 2002). Dessa forma, o jovem deve reconhecer o valor das ciências da natureza, especialmente da química, pela busca do conhecimento da realidade objetiva e se utilize dele no seu cotidiano. Para isso, ele poderá vivenciar de forma investigativa esses elementos, por meio de temas de seu cotidiano como, por exemplo, os aromas e as fragrâncias. Dessa forma, uma sugestão ao professor de Química é que ele poderá utilizar os temas abordados neste trabalho como Tema Gerador para uma abordagem contextualizada de conteúdos relacionados à área da Química Orgânica, especialmente a função orgânica fenol.
|
Por meio do exposto anteriormente, foi possível observar que a vanilina é uma molécula de suma importância, estando presente sob várias formas em nosso cotidiano. Também foi possível vislumbrar os aspectos relacionados à sua origem e principalmente quanto às formas de produção, em que foi possível classificar a vanilina como natural ou sintética. Foi possível verificar que existe um grande campo a ser explorado no que tange à produção biotecnológica desse aroma, uma vez que as substâncias produzidas por esses processos são consideradas substâncias naturais.
Curiosidades
O que acontece dentro de um corpo apaixonado?
Por que os homens sentem tanta atração pelas pernas femininas?
Pupilas dilatadas, circulação mais rápida, tremores. Como acontecem as reações químicas que chegam com uma paixão intensa?
Por que a voz de um apaixonado muda de tom?
Em um teste infalível, a ressonância revela a inundação de felicidade no cérebro de quem vê a foto do verdadeiro amor.
Feromônio: o cheiro da paixão pode mudar uma vida.
Em um beijo, 29 músculos entram em ação. É uma tempestade de prazer dos pés à cabeça. No carinho, o toque provoca explosões internas.
E na primeira relação sexual, o coração está a 150 batimentos por minuto. Como os hormônios atravessam a medula e transformam o corpo?
Homens e mulheres em busca do parceiro ideal na dança. Como funciona o radar interno que identifica até os músculos debaixo das roupas.
E a ciência agora já sabe quais as características físicas que mais atraem os homens e as mulheres.
Vamos falar então da Química no amor, no beijo, no toque enfim do envolvimento entro dois seres.
A Química do Amor
Imagine um Cupido usando o arco e a flecha impregnados de noradrenalina.
Você já ouviu esta frase: Rolou uma química entre nós! Será que existe mesmo uma explicação científica para o amor?
O sentimento não afeta só o nosso ego de forma figurada, mas está presente de forma mais concreta, produz reações visíveis em nosso corpo inteiro. Se não fosse assim como explicar as mãos suando, coração acelerado, respiração pesada, olhar perdido (tipo "peixe morto"), o ficar rubro quando se está perto do ser amado?
Afinal, o amor tem algo a ver com a Química? Na verdade O AMOR É QUÍMICA! Todos os sintomas relatados acima têm uma explicação científica: são causados por um fluxo de substâncias químicas fabricadas no corpo da pessoa apaixonada. Entre essas substâncias estão: adrenalina, noradrenalina, feniletilamina, dopamina, oxitocina, a serotonina e as endorfinas. Viu como são necessários vários hormônios para sentir aquela sensação maravilhosa quando se está amando?
A dopamina produz a sensação de felicidade, a adrenalina causa a aceleração do coração e a excitação. A noradrenalina é o hormônio responsável pelo desejo sexual entre um casal, nesse estágio é que se diz que existe uma verdadeira química, pois os corpos se misturam como elementos em uma reação química.
Mas acontece que essa sensação pode não durar muito tempo, neste ponto os casais têm a impressão que o amor esfriou. Com o passar do tempo o organismo vai se acostumando e adquirindo resistência, passa a necessitar de doses cada vez maiores de substâncias químicas para provocar as mesmas sensações do início. É aí que entra os hormônios ocitocina e vasopressina, são eles os responsáveis pela atração que evolui para uma relação calma, duradoura e segura, afinal, o amor é eterno!
A ciência explica, mas a vida ensina…
Veja esse video, lá você entenderá melhor como a química do amor acontece dentro de nós.
https://www.youtube.com/watch?
Quer saber mais acesse https://www.brasilescola.com/
Assunto Sugerido: Iara Bubolz granduanda em Química Industrial- Ufpel/RS e Colaboradora.